最近两年,常有客户询问到MDSAP认证相关事宜,申请并通过MDSAP认证对医疗器械出口企业有诸多好处,因此,撰文为大家科普一下。
一、什么是MDSAP认证?
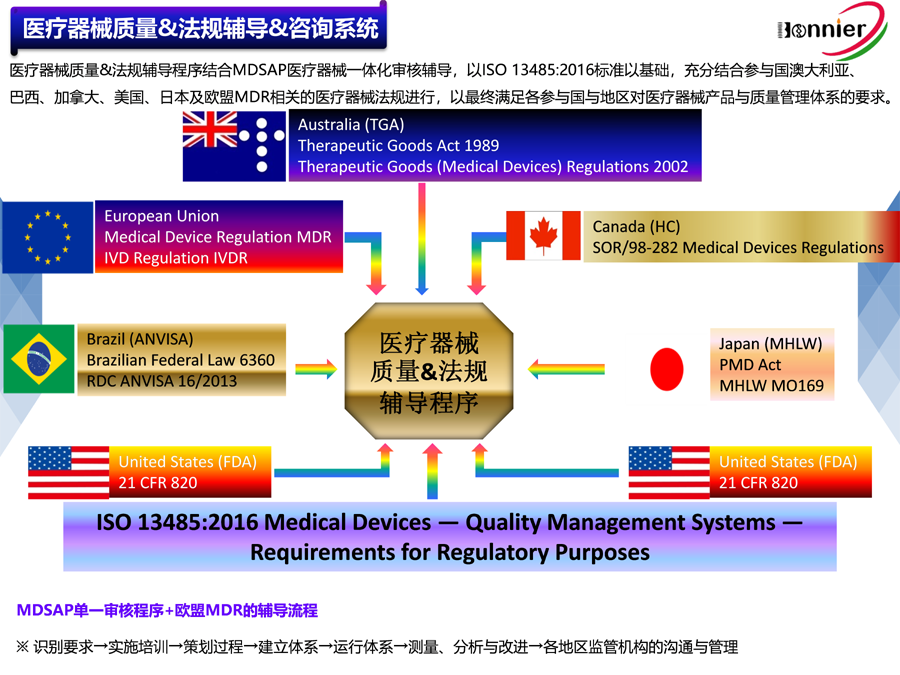
MDSAP是Medical Device SingleAudit Program的英文首字母缩写,翻译成中文习惯叫做“医疗器械单一审核程序”,MDSAP认证项目是美国(FDA)、澳大利亚(TGA)、巴西(ANVISA)、加拿大(HC)、日本(MHLW)五国的监管机构认可并加入的一套新的审核程序。该程序旨在建立一套单一审核的过程,满足并统一上述国家的审核要求,使审核更加全面有效。以上五国监管机构认可MDSAP的审核结果,生产企业可以减少对应不同监管机构的审核次数,减少因审核带来的生产干扰。MDSAP的出台,使审核过程国际标准化,减轻了生产企业的负担。
二、MDSAP认证与ISO13485认证的异同:
ISO13485是MDSAP的基础;MDSAP认证的要求要高于/多于ISO13485的要求;
ISO13485是标准,MDSAP除了ISO13485之外,还有各参与国的法规要求;
ISO13485和MDSAP两种认证,核心都是质量管理体系。
三、申请并通过MDSAP认证的意义:
MDSAP由医疗器械生产企业联系第三方公告机构(如:SGS、BSI、TUV)进行审核,参与国(五国:美国、澳大利亚、巴西、加拿大、日本)的医疗器械监管部门可以将此审核报告作为判断依据。
四、相关国家认可的程度如下:
美国:替代FDA的常规检查(FDA专项和PMA产品除外);
巴西:对于三类和四类医疗器械,可以替代ANVISA的上市前GMP检查,以及上市后的例行检查(专项检查除外);
日本:对于II类,III类,IV类医疗器械,可豁免现场工厂审核;
加拿大:2019年起强制取代CMDCAS,作为分类在II类及以上产品进入加拿大的唯一途径;
澳大利亚:可豁免TGA审核,支持颁发和保持TGA符合性审核证书。
五、企业怎样申请MDSAP认证:
第一步:聘请专业医疗器械第三方服务机构,建立符合MDSAP要求的质量管理体系;
第二步:企业识别MDSAP法规,由质量管理部按照MDSAP的要求进行内审;
第三步:由公告机构到企业进行现场审核;
第四步:企业根据公告机构审核提出的整改项进行整改,15天内提交整改计划;
第五步:公告机构审核企业的整改情况;
第六步:审核通过,公告机构内部走出证审批程序,颁发MDSAP证书。
博尼尔质量管理咨询(江门)中心擅长的业务范围:
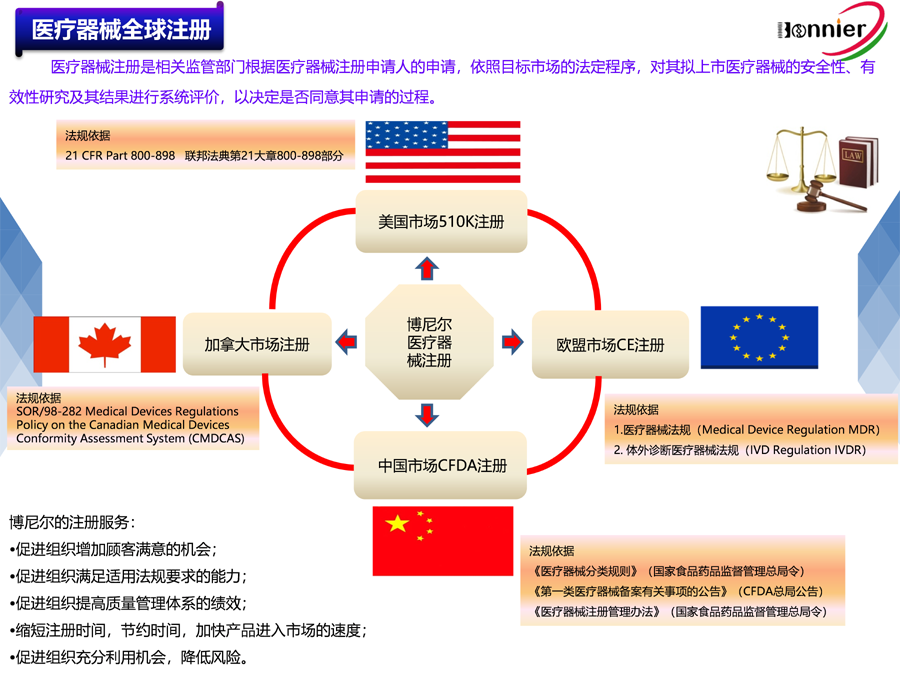
※医疗器械注册咨询服务:
医疗器械FDA 510k咨询辅导;
医疗器械FDA 510k咨询;
医疗器械加拿大MDL注册咨询;
医疗器械MDR CE注册咨询。
※医疗器械质量管理体系咨询辅导服务:
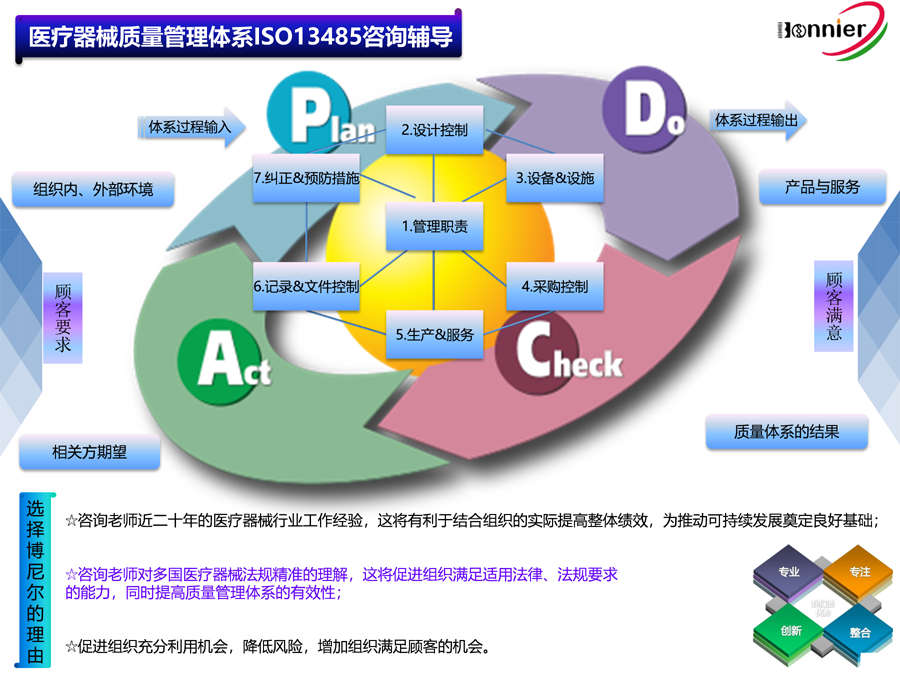
ISO13485咨询辅导;
医疗器械MDR CE咨询辅导;
医疗器械MDSAP认证咨询;
医疗器械QSR820咨询辅导。
※医疗器械授权代表服务:
英国授权代表UKRP;
瑞士授权代表CHREP;
美国代理人FDA Agent;
欧盟授权代表ECREP。