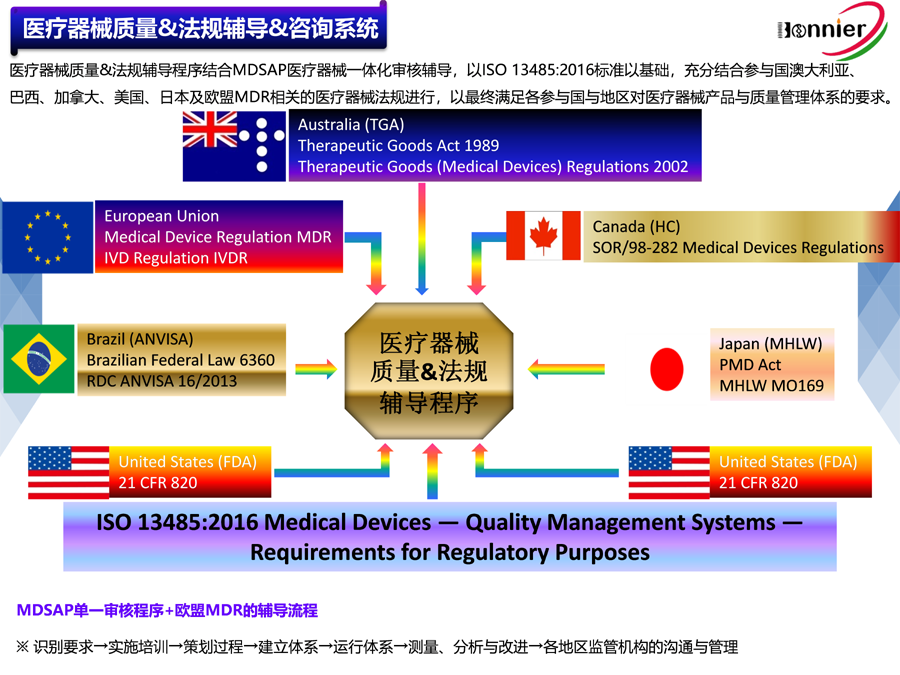
MDSAP医疗器械单一审核程序认证咨询服务是帮助企业通过一次审核满足美国FDA、澳大利亚TGA、巴西ANVISA、加拿大HC和日本MHLW等五国的医疗器械质量管理体系(QMS)和生产质量管理规范(GMP)要求的服务。以下是关于MDSAP认证咨询服务的详细信息:
1.MDSAP认证的意义
MDSAP认证旨在通过一次审核替代多个国家或地区的多次审核,从而减轻企业的合规负担,提高市场准入效率,并增强企业的合规性和透明度。MDSAP认证基于ISO 13485标准,但要求更高,涵盖了各参与国的额外法规要求。
2.申请MDSAP认证的流程
建立质量管理体系:企业需建立符合MDSAP要求的质量管理体系,并准备必要的文件和资料。
内审与整改:企业进行内部审核,识别并整改不符合项,提交整改计划。
现场审核:由经过IMDRF认可的第三方审核机构进行现场审核。
监督审核与再认证:证书有效期三年,每年需进行监督审核,第三年进行再认证审核。
3.MDSAP认证的优势
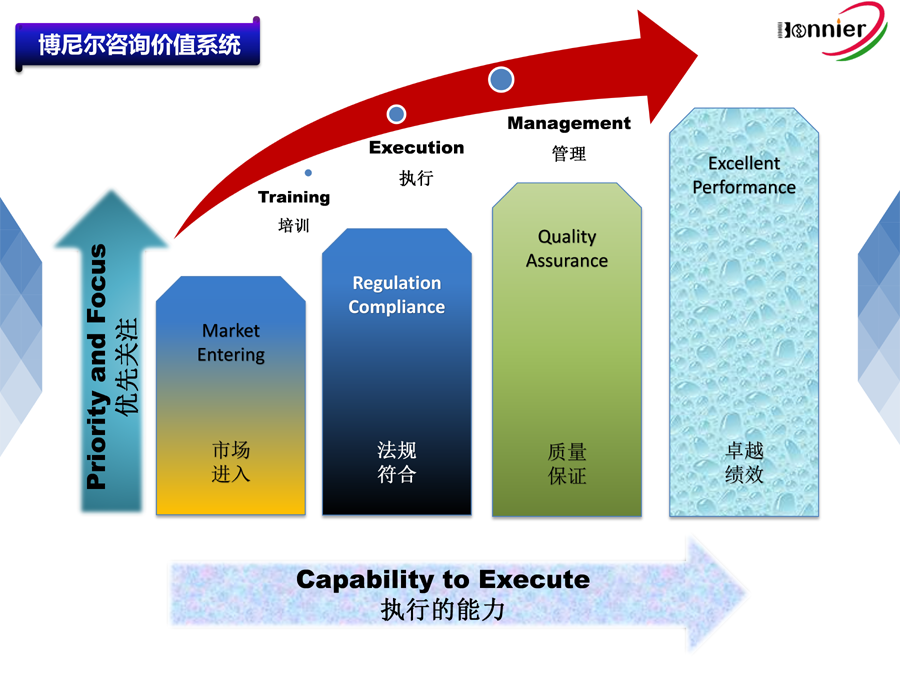
减少审核次数和成本:通过一次审核满足多个国家或地区的监管要求,显著降低企业的审核成本和时间压力。简化市场准入:MDSAP认证结果被五国监管机构认可,企业可以更快速地进入国际市场。提高合规性和透明度:确保企业在全球范围内的生产和运营符合高标准的质量管理体系要求,提升企业形象和客户信任度。
4.MDSAP认证咨询服务内容
体系建立与优化:帮助企业建立或优化符合MDSAP要求的质量管理体系。
法规咨询与培训:提供MDSAP相关法规的咨询和专项培训服务。
模拟审核与陪审:通过模拟审核帮助企业识别薄弱环节,并提供现场陪同审核服务。
整改指导与证书维护:协助企业完成整改并维护MDSAP证书的有效性。
5.选择MDSAP认证服务的机构
企业可以选择专业的第三方服务机构,如TUV、SGS、UL Solutions、博尼尔质量管理咨询(江门)中心等,这些机构提供从体系建立到认证申请的全流程服务。此外,一些机构还提供定制化的MDSAP认证服务,以满足企业的具体需求。MDSAP认证咨询服务为企业进入国际市场提供了高效、经济的解决方案,通过专业的辅导和支持,企业可以顺利完成MDSAP认证,实现多国市场的合规准入。
博尼尔质量管理咨询(江门)中心擅长的业务范围:
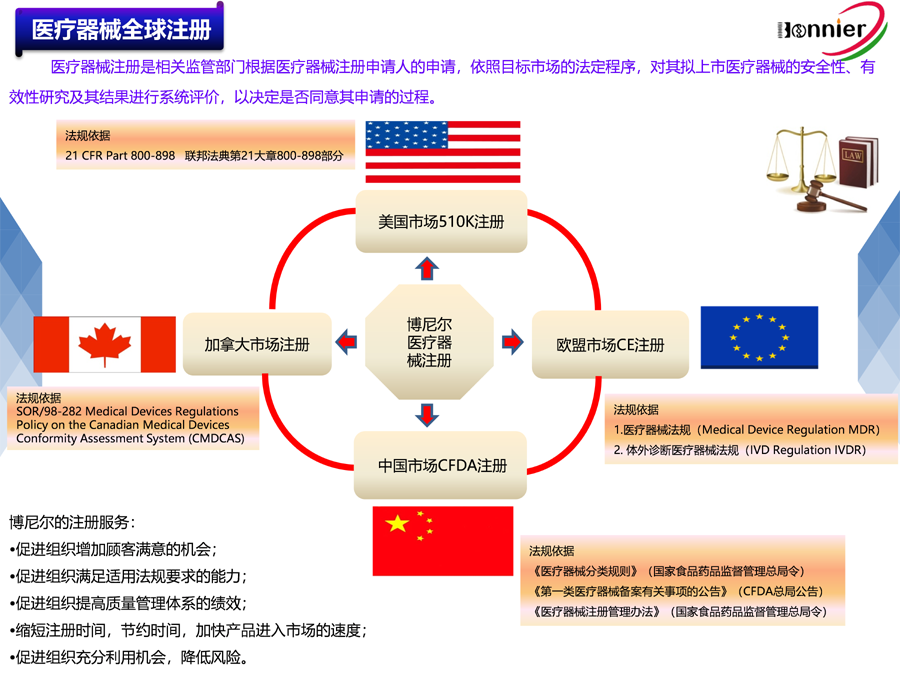
※医疗器械注册咨询辅导服务
医疗器械美国FDA 510k注册咨询服务;
医疗器械加拿大HC MDL注册咨询服务;
医疗器械澳大利亚TGA注册咨询服务;
医疗器械欧盟CE注册咨询服务。
※医疗器械法规&质量管理体系咨询辅导服务:
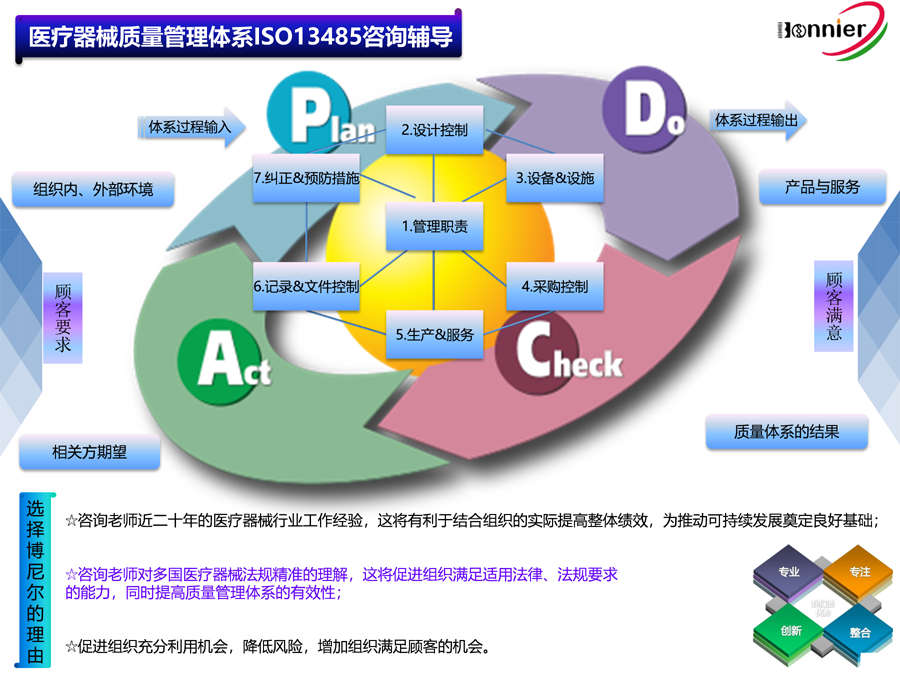
ISO13485医疗器械质量管理体系认证咨询辅导服务;
医疗器械欧盟MDR745认证咨询辅导服务;
医疗器械欧盟IVDR746认证咨询辅导服务;
医疗器械MDSAP认证咨询服务;
医疗器械美国QSR820咨询辅导服务。
※医疗器械授权代表服务:
英国授权代表UKRP;
瑞士授权代表CH REP;
美国代理人FDA Agent;
欧盟授权代表EC REP。